广泛期小细胞肺癌(ES-SCLC)是一种预后极差的高度恶性肿瘤,疾病进展不可避免,目前复发的患者治疗选择仍然十分有限!山东省肿瘤医院王哲海教授带领团队进行了信迪利单抗联合安罗替尼和化疗作为复发ES-SCLC患者二线或后线治疗的II期临床试验。该研究除展示了联合方案的有效性和安全性外,进一步使用艾德生物Master Panel进行了循环肿瘤DNA (ctDNA)探索性生物标志物分析,发现治疗过程中低bTMB状态可筛选出广泛期小细胞肺癌三药联合治疗潜在获益人群,提示了ctDNA中KMT2D突变可用于鉴定三药联合治疗潜在原发耐药的患者。此外,通过联合小细胞肺癌细胞系与公共多组学数据揭示了KMT2D突变广泛影响了表观遗传修饰过程,与免疫抑制性微环境特征显著相关,为开发新的联合治疗策略提供了重要的理论依据。该成果于近日发表在Signal Transduction and Targeted Therapy(IF 40.8)期刊上,并获得了审稿专家的高度评价。

 图1:审稿专家高度评价了ctDNA生物标志物探索性分析的结果与科学意义
图1:审稿专家高度评价了ctDNA生物标志物探索性分析的结果与科学意义
该项II期临床试验(ChiCTR2100049390)于2021年7月15日至2023年4月4日期间最终筛选入组了25例既往至少接受过一次全身治疗的ES-SCLC患者,患者进行6个周期(每周期21天)的联合方案治疗(信迪利单抗、安罗替尼和nab-紫杉醇),随后信迪利单抗维持治疗,主要研究终点为ORR。
基于ctDNA的探索性分析:分别在第1周期第1天(C1D1,治疗前)和第2周期第1天(C2D1,治疗中)采集参与者的血液样本,使用艾德生物Master Panel产品进行ctDNA测序。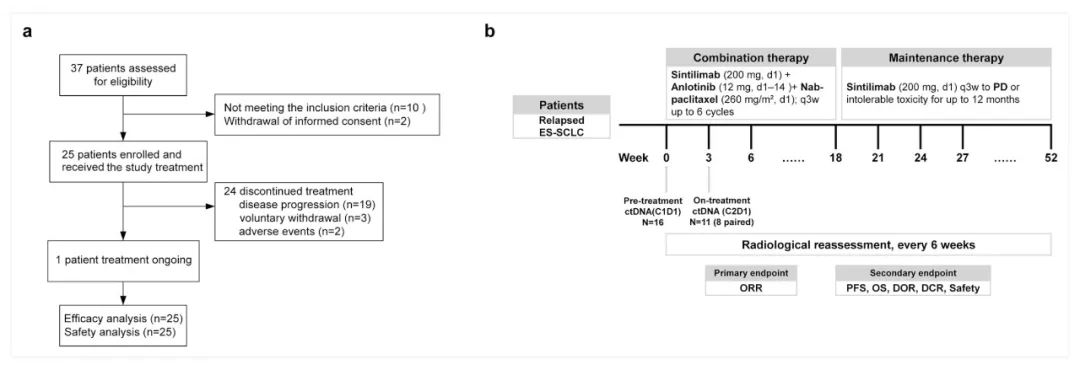
图2:参与者流程图和试验计划
☆联合疗法作为ES-SCLC的二线或后线治疗显示出良好的疗效与可控的安全性
患者中位随访时间为13.0(范围3.0-30)个月,15例患者为部分缓解(PR),4例疾病稳定(SD),ORR为60% (95% CI: 38.7-78.9%),疾病控制率(DCR)为76% (95% CI: 54.9-90.6%)。中位缓解时间为1.9个月(95% CI: 1.57-NA),中位反应持续时间(DOR)为5.2 (95% CI: 4.1-11.7)个月,最长为19.3个月。中位无进展生存期(mPFS)为6.0 (95% CI: 5.4-9.7)个月,6个月PFS率为49.2%。中位总生存期(mOS)为13.4个月(95% CI: 11.8-NR),12个月生存率为62.2%。80%的患者发生了任一级别的治疗相关不良事件(TRAEs),最常见的是疲劳(40%)和恶心(32%),12%的患者具有3级或更高级别的TRAEs。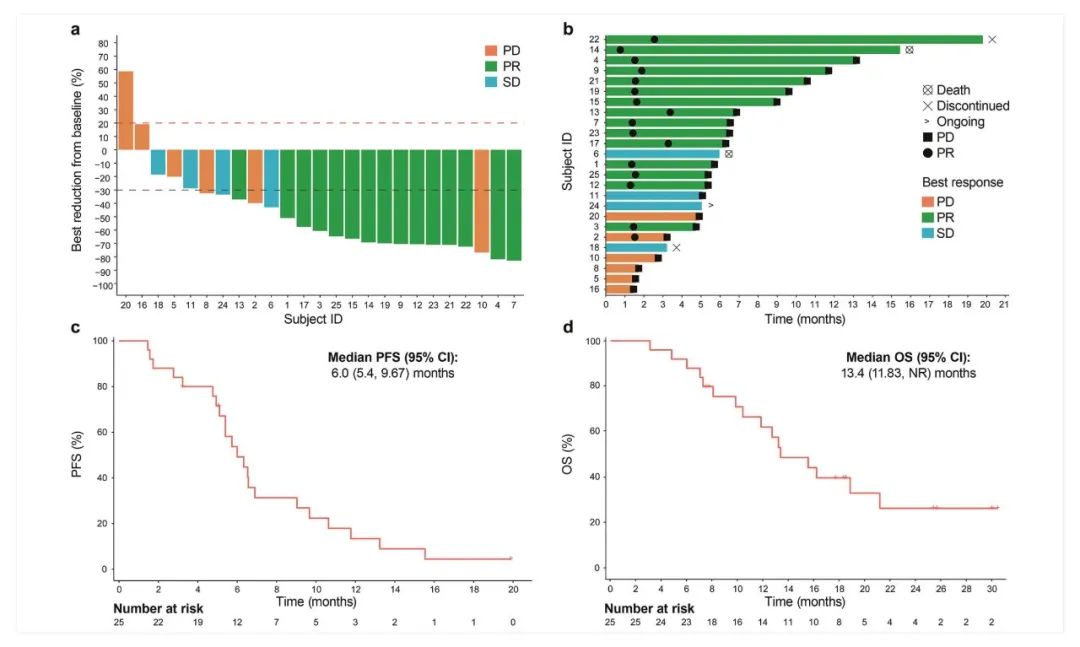
ctDNA图谱特征与患者治疗响应和长期生存:较低的治疗中bTMB与较长的PFS和OS相关,KMT2D突变是潜在的耐药机制。研究分析了27份外周血样本,包括预处理期间收集的16份样本和第一个治疗周期后获得的11份样本。结果显示,最常发生突变的基因包括TP53(88%)、MUC16(56%)、RB1(44%)、DNMT3A(31%)、ZFHX4(31%),这些突变与先前报道一致(图4a)。研究发现ctDNA中KMT2DMUT(突变型)对免疫联合治疗存在负向影响,风险比(HR)为4.103。生存分析显示KMT2DMUT小细胞肺癌患者的PFS较短。这些结果表明KMT2D突变为潜在的耐药机制(图4b,c)。研究进一步发现治疗中bTMB水平与良好的治疗效果相关。生存分析显示治疗中低bTMB水平的患者的PFS (Log-rank P = 0.034)和OS (Log-rank P = 0.005)显著改善,表明治疗中低bTMB水平可作为治疗疗效的预测生物标志物(图4b,d)。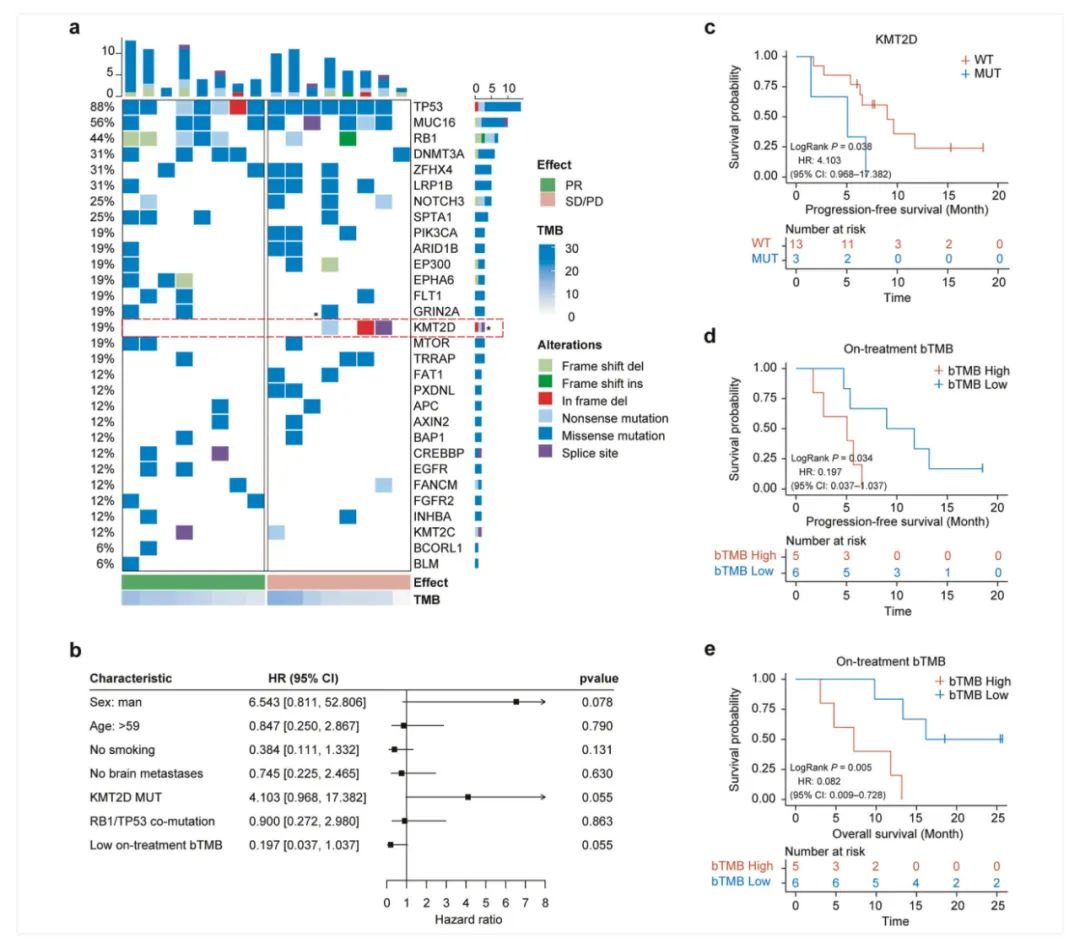
KMT2D突变影响了MLL4蛋白表达和表观遗传修饰、细胞分裂相关通路,为潜在干预策略提供了新的方向研究对KMT2DMUT(突变型)和KMT2DWT(野生型)亚组之间的KMT2D/MLL4蛋白水平进行了比较,发现KMT2DMUT组的KMT2D/MLL4蛋白水平显著降低。通路富集分析揭示了KMT2D突变影响的关键途径包括组蛋白甲基化,H3K9三甲基化(基因沉默的关键标记)、染色质分解和蛋白质-DNA复合物分解。研究还发现KMT2DMUT小细胞肺癌细胞中表观遗传修饰的关键蛋白(包括MEN1和SUZ12,SWI/SNF复合体成员蛋白,SMARCB1/C1/D2, ARID1B/4D等)在表达水平上具有很大的差异,提示KMT2D突变对表观遗传修饰和调控存在显著且广泛的影响。此外,细胞周期调控、DNA复制和染色体分离等细胞分裂的通路活性在KMT2DMUT细胞中明显增强。当KMT2D突变存在时,参与细胞有丝分裂的蛋白(如NUMA1、SMG6和TTK)和Notch/ephrin/ neurotrophin信号通路相关蛋白(JAG1和ROBO1)发生了显著上调。这些蛋白质的显著差异改变可有助于开发针对性的治疗策略(图5)。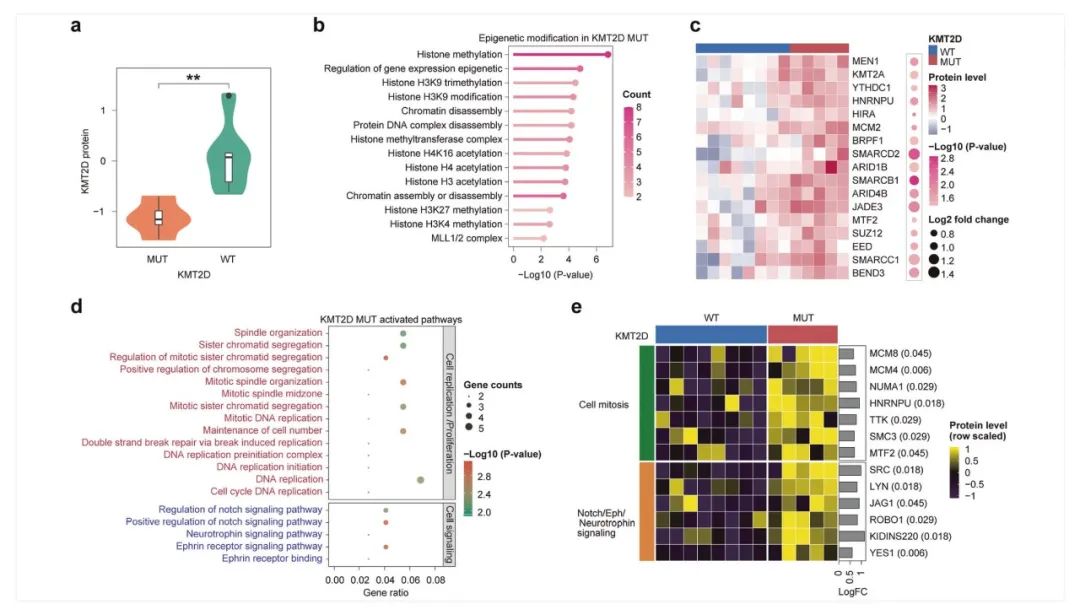
KMT2D突变降低了小细胞肺癌的凋亡途径,并抑制了抗肿瘤免疫活性研究发现KMT2DMUT细胞中凋亡途径和免疫应答通路被显著抑制。在KMT2DMUT细胞中,关键凋亡相关蛋白如PML、TRADD、HSPA1A和HSPB6显著下调。此外,抗原加工和递呈途径(包括关键蛋白CD74和SAR1B)以及炎性细胞浸润显著下调,免疫调节性细胞的浸润显著增加,提示了KMT2DMUT小细胞肺癌潜在的免疫逃逸机制。KMT2D突变影响了肿瘤微环境中的多种免疫细胞浸润,其特征为促炎细胞浸润减少和免疫调节细胞增加(图6)。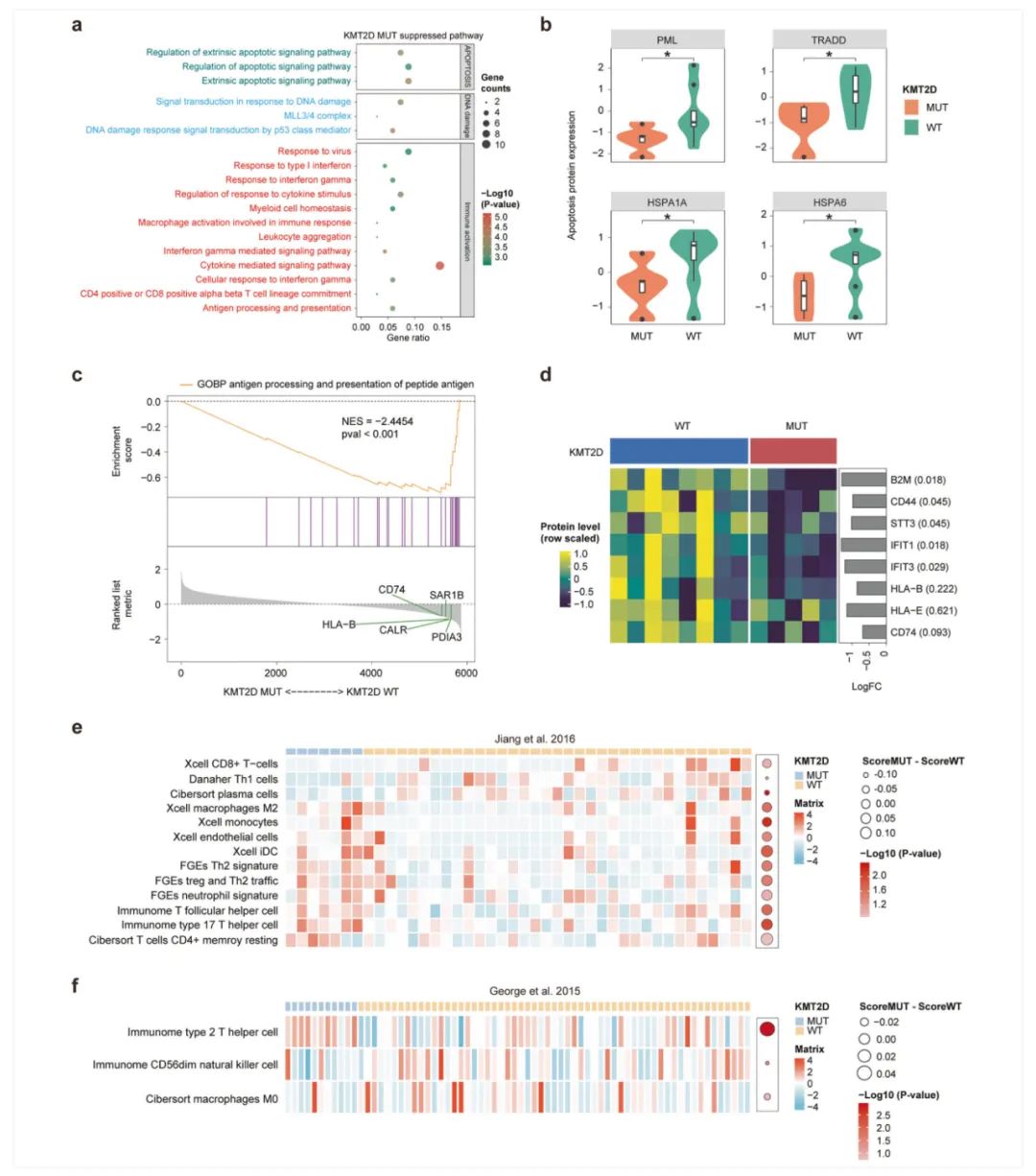
图6:KMT2D突变对免疫和细胞通路影响的综合分析
该研究首次报道了信迪利单抗联合安罗替尼和化疗治疗复发性SCLC患者的临床研究结果,在二线或后线治疗中,患者ORR高达60%,而既往复发SCLC患者的疗法ORR通常低于50%。安罗替尼具有改变肿瘤微环境使其更有利于免疫治疗,以及通过血管正常化改善药物递送的作用,化疗药物既往研究提示具有免疫增强作用,所以该研究能够获得良好的疗效可能是三种药物协同作用的结果。
本次研究基于ctDNA分析提供了很多有价值的数据,低治疗中bTMB与临床治疗结果改善相关,KMT2D基因突变为治疗产生耐药的重要潜在因素。KMT2D基因突变相关的肿瘤免疫系统相互作用、免疫逃逸和细胞凋亡减少可能促成了对治疗的耐药性。而且研究结果还揭示了携带KMT2D突变的细胞中NOTCH/ Eph和神经营养因子通路上调,为治疗干预提供了新的潜在靶点!
该项研究中信迪利单抗联合安罗替尼和化疗治疗方案刷新了复发性SCLC患者的临床获益,ORR为60%,DCR为76%,为这一难以治疗的患者群体带来了希望,且安全性可控。尤其是基于ctDNA探索性分析为这种联合治疗的潜在生物标志物提供了重要的见解。为了全面分析复发性SCLC患者的ctDNA谱,以探讨其与治疗反应和生存结果的关系,该研究对治疗前和第一个治疗周期后的血液样本进行检测,分析结果表明,较低的治疗时bTMB与较长的PFS和OS相关,KMT2D基因突变是治疗产生耐药的重要潜在因素。而且强调了与KMT2D突变相关的广泛的表观遗传修饰,特别是影响H3K4、H3K9和H3K27的组蛋白甲基化,这可能潜在地调节肿瘤微环境以促进免疫逃逸,从而降低免疫治疗疗效。这些研究发现为复发性SCLC的治疗前景提供了革命性的见解,有望提高患者的预后。

 图1:审稿专家高度评价了ctDNA生物标志物探索性分析的结果与科学意义
图1:审稿专家高度评价了ctDNA生物标志物探索性分析的结果与科学意义







